Services mondiaux
Identifiant unique de dispositif (UDI)
Le 24 septembre 2013, la Food and Drug Administration (FDA) des États-Unis a publié une règle finale exigeant que la plupart des dispositifs médicaux distribués aux États-Unis soient munis d’identifiants uniques de dispositif (UDI). Le système UDI facilite l’identification, la traçabilité et le suivi des dispositifs médicaux tout au long de leur distribution et de leur utilisation. La règle exige que les informations relatives aux dispositifs soient soumises à la Base de données mondiale des identifiants uniques de dispositifs (GUDID) de la FDA.
De plus, la règle impose également l’utilisation d’un nouveau format de date standardisé sur toutes les étiquettes de dispositifs médicaux.
Masimo a mis à jour nos étiquettes afin de se conformer à la réglementation UDI et aux normes GS1.
Si vous avez des questions ne relevant pas de cette FAQ, veuillez contacter le service client :
É.-U. : customerorders@masimo.com
En dehors des É.-U. : emeasales@masimo.com
Qu’est-ce que l’UDI ?
Un identifiant unique de dispositif (UDI) est une série de caractères numériques ou alphanumériques, basée sur une norme de codage mondiale, permettant d’identifier de manière précise un dispositif au moment de sa distribution et de son utilisation. L’UDI se compose de :
- Un identifiant de dispositif, le GTIN (Global Trade Item Number) : une portion obligatoire et fixe d’un UDI identifiant la version ou le modèle spécifique du dispositif ainsi que le fabricant de ce dispositif ; et
- Un identifiant de production : une portion conditionnelle et variable d’un UDI qui identifie un ou plusieurs des éléments suivants lorsqu’elle figure sur l’étiquette du dispositif :
- Le lot ou la série de production dans lequel le dispositif a été fabriqué ;
- Le numéro de série d’un dispositif spécifique ;
- La date de péremption d’un dispositif spécifique ; et/ou
- La date de fabrication d’un dispositif spécifique.
Masimo utilise GS1 comme organisme accrédité pour l’attribution des codes-barres et définir leur structure.
Veuillez noter que tout produit qui n’est PAS classé comme dispositif médical n’est pas tenu de comporter un code-barres.
2. Qui doit se conformer à la réglementation UDI ?
Toutes les entreprises de dispositifs médicaux doivent se conformer à la réglementation UDI.
3. Quel est le calendrier de mise en œuvre pour se conformer à la réglementation UDI ?
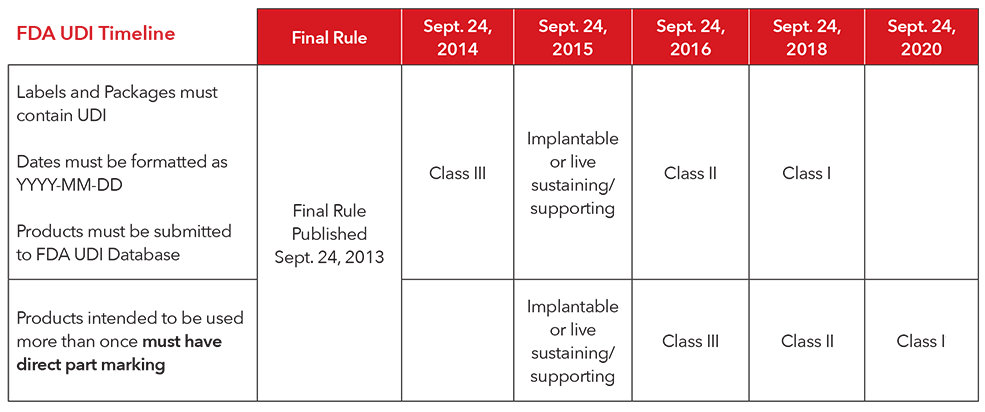
4. Comment Masimo respectera la réglementation UDI ?
Masimo distribue des produits de classe II ainsi que quelques produits de classe I. Masimo a mis à jour nos étiquettes afin de se conformer à la réglementation UDI et aux normes GS1.
Veuillez noter que tout produit qui n’est PAS classé comme dispositif médical n’est pas tenu de comporter un code-barres.
5. À quoi ressembleront mon étiquette UDI et le marquage direct sur la pièce ?
Ci-dessous, des exemples :
- Étiquettes de boîtes de capteurs : version précédente et étiquettes UDI mises à jour
- Capteur avec marquage direct sur la pièce
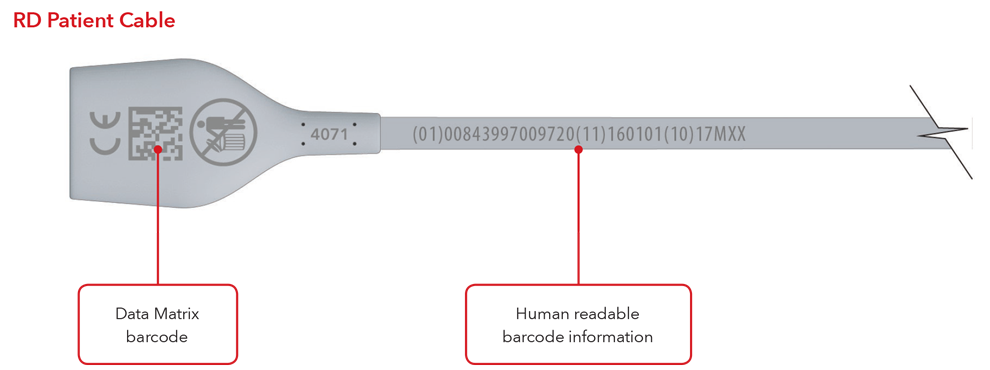
- Câble avec marquage direct sur la pièce
Remarque : selon le type de produit, l’étiquette contiendra l’une des deux dates. Pour les produits comportant une date de « péremption », celle-ci sera indiquée sous le format AAAA-MM-JJ sous le symbole d’expiration. Elle sera également codée sous le format AA-MM-JJ précédée de l’identifiant de production (17) dans les codes-barres GS1 et 2D. Pour les produits ne comportant pas de date de « péremption », la date de fabrication sera indiquée sous le format AAAA-MM-JJ à côté du symbole de date de fabrication. Elle sera également codée sous le format AA-MM-JJ précédée de l’identifiant de production (11) dans les codes-barres GS1 et 2D.
Exemples d’étiquettes de boîtes de capteurs
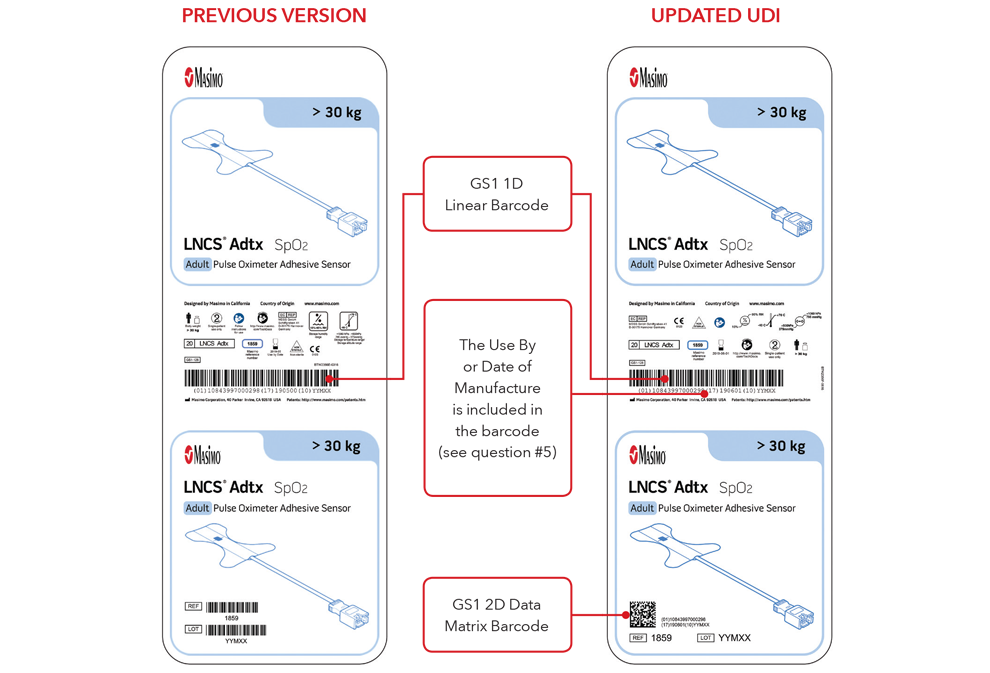
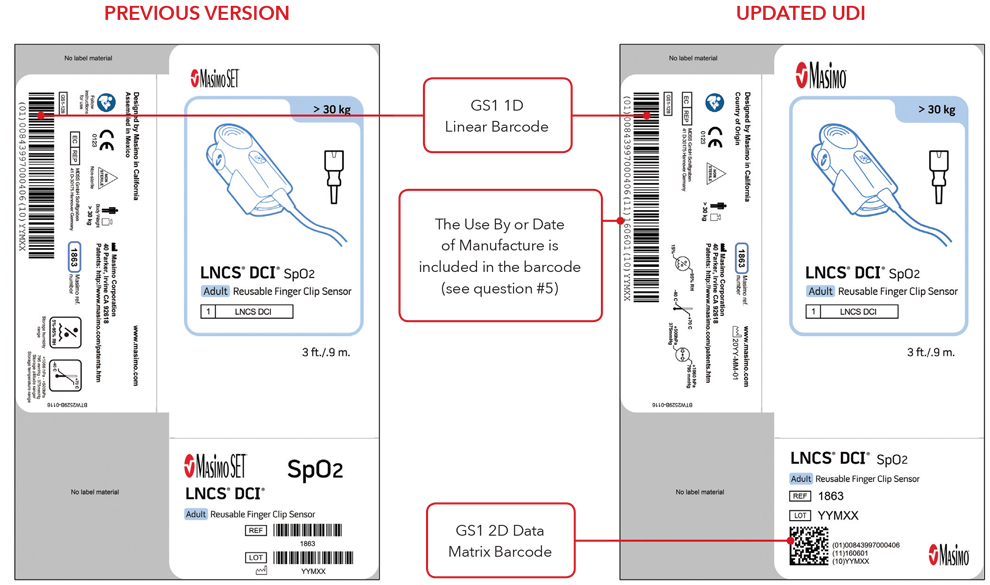
Exemples de capteurs et câbles avec marquage direct sur la pièce
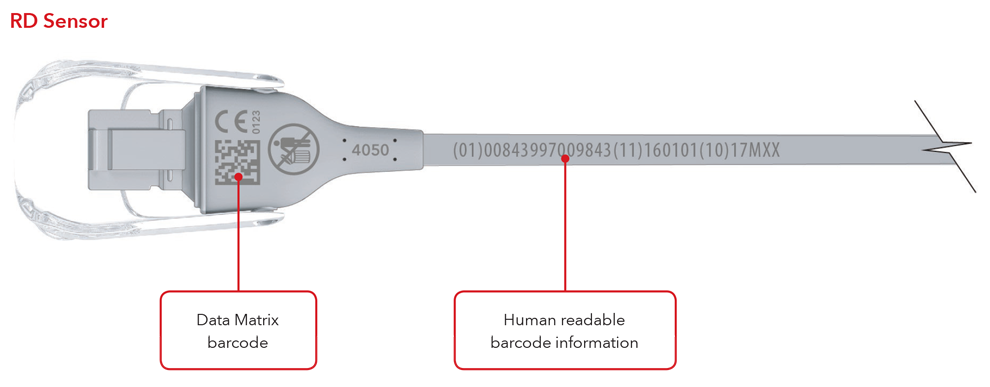
6. Qu’est-ce qu’un Global Trade Item Number (GTIN) ?
Un GTIN est un numéro d’identification GS1 unique au niveau mondial, utilisé pour identifier un « article commercial ». Les GTIN sont attribués par le propriétaire de la marque (fabricant ou étiqueteur) du produit et servent à identifier les produits tout au long de la chaîne d’approvisionnement mondiale jusqu’à l’utilisateur final, comme un hôpital. Si vous n’utilisez pas actuellement le système GS1 avec des GTIN pour gérer vos produits, vous devrez obtenir les GTIN correspondants pour les produits que vous achetez.
Pour en savoir plus sur les GTIN, veuillez contacter GS1 : https://www.gs1us.org/what-we-do/standards.
7. Comment obtenir les GTIN de mes produits ?
Envoyer un e-mail au service client de Masimo :
É.-U. : customerorders@masimo.com
En dehors des É.-U. : emeasales@masimo.com
Veuillez inclure votre identifiant client ainsi que le ou les références des produits dans l’e-mail.
8. Je suis en train de saisir ou de scanner les codes-barres LOT et/ou REF de Masimo figurant sur l’étiquette. Dois-je m’attendre à des interruptions ?
Oui. Les codes-barres LOT ou REF présents sur l’étiquette seront supprimés et remplacés par du texte, et ne pourront plus être scannés. Pour les informations de LOT, vous devrez soit scanner le code-barres GS1, soit le repérer à côté du symbole LOT sur l’étiquette. Les informations REF peuvent être identifiées dans le GTIN correspondant. Pour plus d’informations sur les GTIN, voir la question n°6 ci-dessus.
9. Les numéros de produits Masimo vont-ils changer avec la mise en place de l’étiquetage UDI ?
Non, les numéros de produits Masimo resteront les mêmes.
10. Quel est le nouveau format de date standardisé et quand entrera-t-il en vigueur ?
La règle UDI a adopté le format de date standardisé AAAA-MM-JJ pour les étiquettes des dispositifs. Les dates figurant sur les étiquettes seront dans le nouveau format au plus tard à la date à laquelle l’étiquette du dispositif devra porter un UDI. Pour plus d’informations sur le calendrier de mise en œuvre, voir la question n°3 ci-dessus.
11. Masimo fournira-t-il des informations sur les produits en ligne ?
Le GUDID est une base de données consultable publiquement, qui contient la partie « identifiant de dispositif » de l’UDI pour chaque dispositif médical, ainsi que d’autres informations produits requises. Toutes les entreprises de dispositifs médicaux doivent soumettre les informations relatives à l’identifiant de dispositif au GUDID. Masimo a commencé à alimenter le GUDID et veillera à ce que tous les produits y soient ajoutés conformément au calendrier de mise en œuvre de l’UDI ou même avant celui-ci.
12. Qu’en est-il des stocks existants ? Les fabricants doivent-ils refaire le marquage ?
Non, il existe deux exceptions pour les stocks existants :
- Les dispositifs déjà en distribution commerciale avant la date de conformité applicable n’ont pas à se conformer à la règle finale.
- Les dispositifs fabriqués et étiquetés avant la date de conformité applicable sont également exemptés de cette obligation. Cependant, cette exception expire trois ans après la date de conformité applicable.
13. Tous les dispositifs doivent-ils être marqués directement avec leur UDI ?
Non. La règle exige uniquement le marquage direct pour les dispositifs médicaux réutilisables nécessitant un retraitement (nettoyage/stérilisation de haut niveau) avant réutilisation.
Pour plus d’informations sur le calendrier de mise en œuvre du marquage direct, voir la question n°3 ci-dessus.
Pour plus d’informations sur le système UDI, consultez la page « Unique Device Identification » (UDI) sur le site de la FDA :
http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/UniqueDeviceIdentification/
Si vous avez des questions supplémentaires sur la manière dont Masimo se conforme à la réglementation UDI, veuillez contacter le service client Masimo à l’adresse suivante :
É.-U. : customerorders@masimo.com
En dehors des É.-U. : emeasales@masimo.com
PLCO-008044/ PLMM-12787A-0326 EN- PLMM-10045D